2021年2月19日
ポイント
●生理活性ペプチドのカルボキシル末端アミノ酸の立体構造を反転する新規酵素を発見。
●新規酵素を用いて天然には存在しない新規D-アミノ酸含有ペプチド化合物の創製に成功。
●立体構造の改変により生理活性ペプチドの安定性や生理活性の向上への貢献に期待。
概要
北海道大学大学院工学研究院の大利 徹教授,小笠原泰志准教授らの研究グループは,生理活性ペプチド抗生物質の生合成に関わる新奇なペプチド立体反転酵素を発見しました。
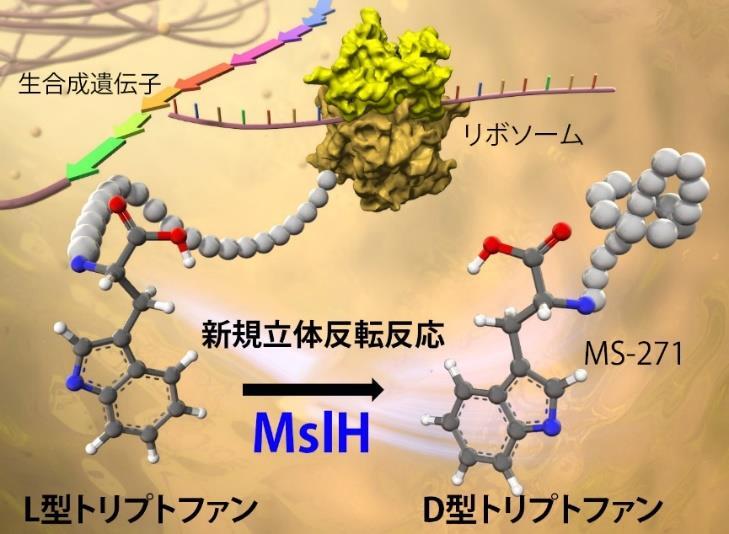
微生物が生産し,抗菌活性や抗腫瘍活性などの有用生理活性を有する低分子ペプチド化合物の中には,タンパク質の翻訳合成系であるリボソームを利用して生合成されるものが存在します。これらのリボソームペプチドは,タンパク質性のアミノ酸を原料に用いて生合成されるため,通常全てのアミノ酸残基がL型の鏡像異性体で構成されます。しかし,ストレプトミセス属放線菌が生産するペプチド抗生物質MS-271は,リボソームペプチドであるにも関わらず,構成する21アミノ酸残基のうちカルボキシル末端のトリプトファンがD型です。
研究グループは,MS-271のD体アミノ酸残基の導入機構に注目し,その解明を目指して研究を進め,鍵反応となる新規のペプチド立体反転酵素(MslH)を突き止めました。本酵素は,既存の酵素と配列類似性が全くなく,ペプチドのカルボキシル末端のアミノ酸残基をL型からD型に変換する初めての酵素です。さらに,得られた結果に基づいて,天然には存在しない新規D-アミノ酸含有ペプチド化合物の創製にも成功しました。
今後,今回見出したペプチド立体反転酵素を自在に使いこなすことで,医薬品など生理活性ペプチドの創製への応用が期待できます。
なお,本研究成果は,化学系トップジャーナルの一つであるChemical Science誌に2020年12月29日(火)にオンライン公開されました。
詳細はこちら