シリーズ「人獣共通感染症との戦い」の第二回。本シリーズでは、人獣共通感染症をはじめ、その他の新興・再興感染症を制御する北海道大学の取り組みを紹介していきます。
喜田 宏(獣医学博士)
・北海道大学 ユニバーシティプロフェッサー
・人獣共通感染症国際共同研究所 特別招へい教授 統括
・WHO 指定人獣共通感染症対策研究協力センター長
人獣共通感染症の克服に向けた研究の第一人者である喜田宏教授は、鳥インフルエンザ、パンデミックインフルエンザや季節性インフルエンザに関する自身の見解に対して、しばしば、誤解に基づくと思われる反発を受けることがあるといいます。そんな時は、個別に反論せず、地道に科学的真実の究明に集中することを心掛けていると話します。
「時には、100対1で意見が分かれることがあります。でも、感染症を克服するには、コツコツと地道に研究を続けるしかない。10年あるいはもっと後には、真実が明らかになるものです」。
不活化ウイルス全粒子ワクチンの実用化に向けて
喜田教授は、インフルエンザウイルスの自然宿主の特定や、ヒトのパンデミックインフルエンザウイルスおよび高病原性鳥インフルエンザウイルスの出現機構を解明した功績で世界的に評価されています。近年、特に注力しているのが、安全で、効果が高く、パンデミックの際にも有効なインフルエンザワクチンの開発です。現在のインフルエンザワクチンの主流は、エーテルまたは界面活性剤でウイルスを分解した「スプリットワクチン」ですが、それより効果が高く安全な「高度精製不活化ウイルス全粒子ワクチン」が理想であると主張しています。現在進行中の臨床試験では、不活性化ウイルス全粒子ワクチンを現行のスプリットワクチンと比較しています。
主張の背景には、武田薬品工業に技術研究職として勤務していた1970年に、高純度不活化ウイルス全粒子ワクチンの開発・実用化に成功した経験があります。「現在行なっている臨床試験で、全粒子ワクチンの有効性と安全性が確認されています。より少ないウイルス原材料で十分な免疫を誘導することに加えて、ウイルスを破壊する必要がないので、より安価にワクチンを製造することができます」。
2015年から、日本のインフルエンザワクチンメーカー全5所・社と不活化全粒子ワクチンの開発・実用化に向け、産学官共同プロジェクトを開始。国立感染症研究所も同プロジェクトに参加し、日本医療研究開発機構(AMED)の助成金により研究開発を進めています。喜田教授は「失敗は許されません」と、社会実装への決意を述べています。
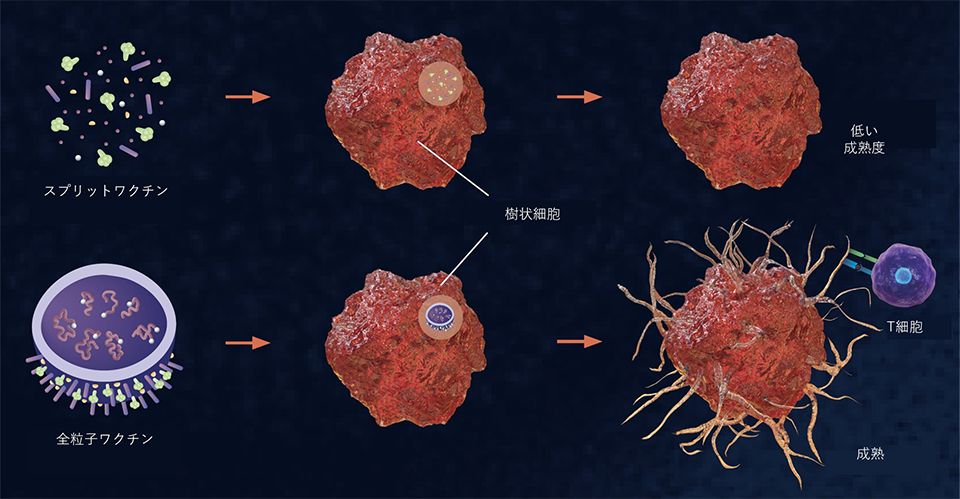 スプリットワクチンと全粒子ワクチンの違い。全粒子ワクチン(下)はウイルスを構成するすべての抗原が樹状細胞に取り込まれ、かつ、遺伝子RNAが樹状細胞を活性化するので、強い免疫を誘導する。
スプリットワクチンと全粒子ワクチンの違い。全粒子ワクチン(下)はウイルスを構成するすべての抗原が樹状細胞に取り込まれ、かつ、遺伝子RNAが樹状細胞を活性化するので、強い免疫を誘導する。一方、スプリットワクチン(上)はHA糖タンパク質の一部のみが未成熟の樹状細胞に取り込まれ、樹状細胞を活性化しないので、免疫誘導能が全粒子ワクチンに比べて低い。
インフルエンザウイルスの自然宿主と伝播経路の解明
喜田教授は1969年4月から武田薬品工業で7年間、インフルエンザなどのワクチンの開発と製造に携わりました。1976年2月に退社し、パンデミックインフルエンザウイルスの出現機構を解明するために、北海道大学の講師として着任しました。その後、A型インフルエンザウイルスの自然宿主がカモであることを特定し、その伝播経路を解明しました。それによると、渡り鳥であるカモは、夏の営巣地であるシベリア、カナダ、アラスカの湖沼で過ごすなかで、A型インフルエンザウイルスに水系で経口感染します。ウイルスは、カモには何の危害も与えませんが、結腸上皮細胞に感染、増殖し、フンとともに排泄されます。A型インフルエンザウイルスには、ヘマグルチニン(HA)とノイラミニダーゼ(NA)という2種類のスパイクタンパク質が表面に存在します。カモからは、様々なHAとNA亜型のウイルスが検出されました。
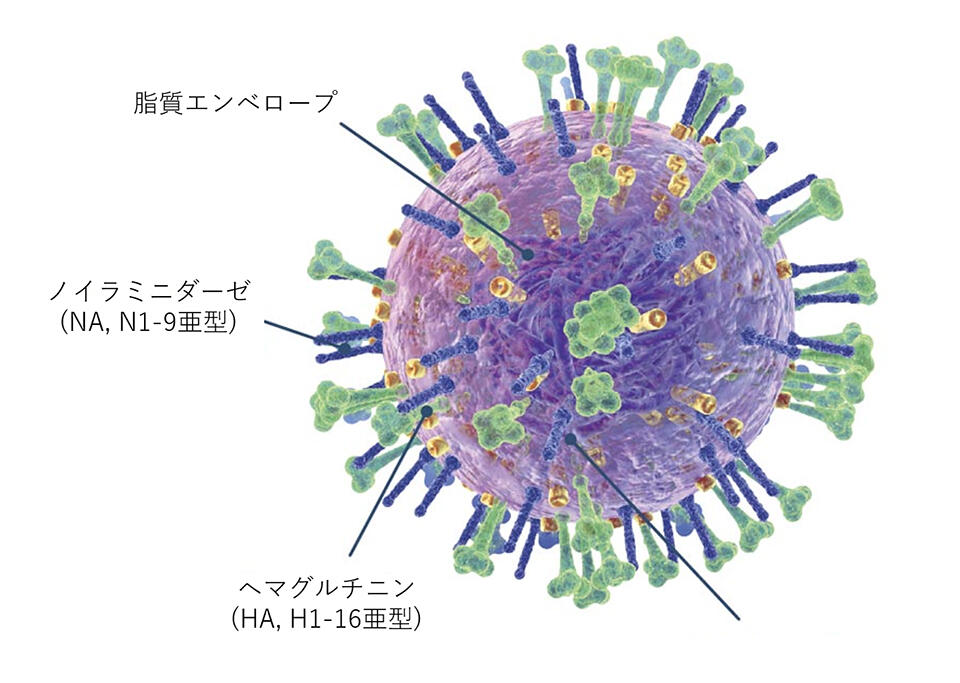 ウイルスの表面にはヘマグルチニン(HA)とノイラミニダーゼ(NA)糖タンパク質突起がある。HAには16の亜型、NAには9の亜型がある。
ウイルスの表面にはヘマグルチニン(HA)とノイラミニダーゼ(NA)糖タンパク質突起がある。HAには16の亜型、NAには9の亜型がある。8月中旬以後に、カモは南方に渡り、中国南部、東南アジア、米国、メキシコでなどの越冬地で過ごします。カモがフンと共に排泄したウイルスは水を介してアヒルやガチョウ、その後、陸鳥であるウズラなどの家禽に感染します。ウズラは、ウイルスの受容体が腸にある水鳥から、受容体が呼吸器にあるニワトリなどの陸鳥にウイルスを伝播する中間宿主の役割を果たします。ウイルスがニワトリの間で6ヶ月から2年間にわたり、どんどん感染を繰り返すと、H5とH7 HA亜型のウイルスは病原性を獲得して、ニワトリに致死性の高病原性鳥インフルエンザを引き起こすことがあります。
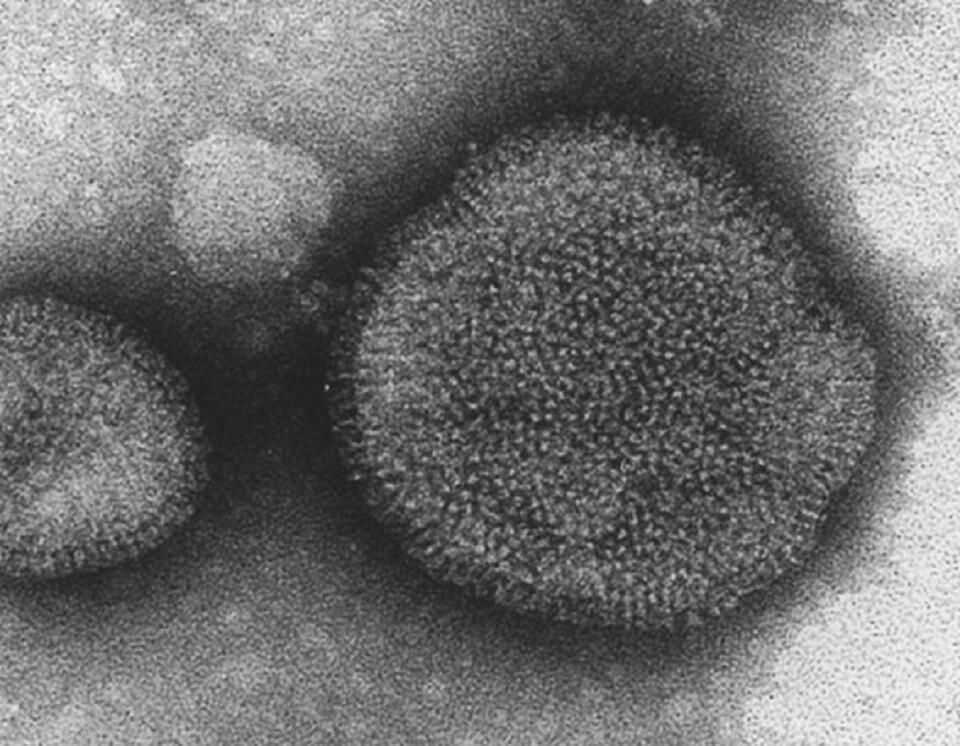 A/duck/Hokkaido/5/77 (H3N2) ウイルスの電子顕微鏡写真<提供:喜田教授、1997年撮影>
A/duck/Hokkaido/5/77 (H3N2) ウイルスの電子顕微鏡写真<提供:喜田教授、1997年撮影>ヒトのパンデミックインフルエンザウイルスは、ヒトの季節性インフルエンザウイルスと鳥インフルエンザウイルスの遺伝子再集合体
ヒトが鳥インフルエンザウイルスに感染することは非常に稀です。また、鳥インフルエンザウイルスのヒトからヒトへの感染も起きておらず、ヒトでパンデミックを起こしたことはありません。では過去のパンデミックインフルエンザである、スペインかぜ(1918年)、アジアかぜ(1957年)、香港かぜ(1968年)、そして2009年のパンデミックインフルエンザはどのように引き起こされたのでしょうか。喜田教授は、ブタの役割を指摘しています。
喜田教授は早くから、インフルエンザが人獣共通感染症ではないかと疑っていました。香港かぜのウイルス株と、アヒルやウマのウイルス株のHAタンパク質に類似性があると指摘する海外の論文を読んでいたからです。1977年10月1日、シベリアから北海道に飛来したカモの腸から、A/duck/Hokkaido/5/77 (H3N2)を分離しました。このウイルスのHAは1968年のパンデミック(香港かぜ)ウイルスのそれとそっくり一致すること、さらにNAは1957年のパンデミック(アジアかぜ)ウイルスのそれとほとんど同じであることが明らかになりました。
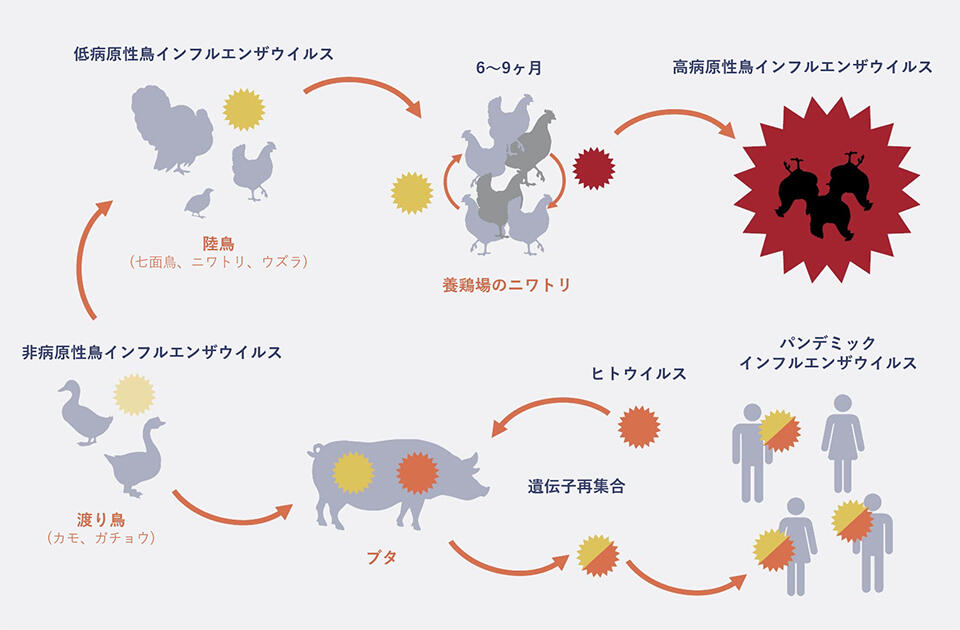 鳥とヒトのウイルス遺伝子再集合体が生まれる仕組み:野生のカモの非病原性鳥インフルエンザウイルスが、ガチョウ、ウズラ、七面鳥などの家禽に感染し、ニワトリに感染する低病原性ウイルスが生じる。このような、ニワトリに対する低病原性ウイルスが、ニワトリ間で6ヶ月~2年以上にわたり感染を繰り返すとニワトリの全身で増殖する高病原性鳥インフルエンザウイルスが優勢となる。
鳥とヒトのウイルス遺伝子再集合体が生まれる仕組み:野生のカモの非病原性鳥インフルエンザウイルスが、ガチョウ、ウズラ、七面鳥などの家禽に感染し、ニワトリに感染する低病原性ウイルスが生じる。このような、ニワトリに対する低病原性ウイルスが、ニワトリ間で6ヶ月~2年以上にわたり感染を繰り返すとニワトリの全身で増殖する高病原性鳥インフルエンザウイルスが優勢となる。ブタの呼吸器上皮細胞に、鳥インフルエンザウイルスとヒトインフルエンザウイルスの両方が同時感染すると、両ウイルスの8遺伝子分節の再集合ウイルスが産生される。遺伝子分節の組み合わせが異なる再集合ウイルスの中で、ヒトに感染して拡がったものがパンデミックウイルスである。
「パンデミックウイルスが生まれるのは、抗原変異ではなく、異なるウイルス株間で起こる遺伝子再集合によることを、このウイルスをシベリアから持って来てくれたカモが教えてくれました」と喜田教授。遺伝子再集合とは、ウイルス間で遺伝子を交換することで、このカモから見つかったウイルスの8つの遺伝子分節のうち2つはカモ由来であり、6つはアジアかぜ由来だということが判明しました。
「我々は、鳥ウイルスとヒトウイルスの両方に感染するブタの役割を実証しました。ブタが両方のウイルスに同時に感染すると、遺伝子再集合が起り、『鳥とヒトのハイブリッドウイルス』ができ、人に感染して広がる。これがパンデミックインフルエンザです」。
伝播性は高いが、病原性は低い
喜田教授は、過去のパンデミックインフルエンザ(1918年のスペインかぜ、1957年のアジアかぜと1968年のホンコンかぜ)はブタの呼吸器で生まれた遺伝子再集合ウイルスによって引き起こされたものと考え、ブタ仲介仮説を唱えていました。折しも2009年にブタインフルエンザウイルス(H1N1)がパンデミックインフルエンザを起こしました。
「いわゆる専門家が『鳥やブタのインフルエンザウイルスがヒトに感染・伝播して、"新型"インフルエンザが発生すると日本だけでも60万人を超える死者が出る』などと、唱えたため、不要な社会不安が煽られました。その結果制定されたのが、新型インフルエンザ等対策特別措置法(2012年~)です」。
「私は同法制定には強く反対しました。『高病原性鳥インフルエンザウイルスがニワトリ間で感染を繰り返すうちに変異を起こしてヒトに"新型"インフルエンザを起こすのは秒読み段階』などの誤った発言がメディアから行政をも誤誘導したことを反省すべきです。また、ブタで増殖したウイルスが、ヒトに感染してすぐには、それほど増殖しませんので、重症者、死者はそれほど多くは出ません。ヒトはパンデミックウイルスに対して免疫を持っていないのでウイルスの伝播性は高いのですが、病原性はそんなに高くないのです。伝播性と病原性を混同してはいけません。パンデミックの第一波より、第二波以後、すなわち季節性インフルエンザの方が恐いのです。季節性インフルエンザ対策を放置して、新型、新型と大騒ぎ、そしてすぐに忘れる。そんなことを繰り返してはいけません。平時こそ、有事に備えることを忘れてはいけません」。
「スペイン風邪は病原性が高く、その結果、4,000万人が死亡した」と言われていますが、死因の多くは細菌感染であり、劣悪な生活環境が背景にあったことが近年の研究でわかっていています。ウイルスは、毒素ではない。病気は、ウイルスの増殖に対する宿主生体の反応であり、激しいウイルス増殖に対する生体の過剰免疫応答が重症化や死亡を起こすと、喜田教授は指摘します。
このように、世の中にはパンデミックインフルエンザについて誤解があると、喜田教授は言います。「『鳥インフルエンザが変異して新型インフルエンザが現れる』などと、不正確に伝えるメディアは多い。そもそも、ウイルス株は変異ウイルスの集合体で、ヒトからヒトへ感染する中で、増殖力が強い変異ウイルスが他のウイルスより優勢になるのです」。また、「パンデミックインフルエンザウイルスは翌年以降、季節性インフルエンザウイルスとなり、病原性が上がるのです」と付け加えてくれました。
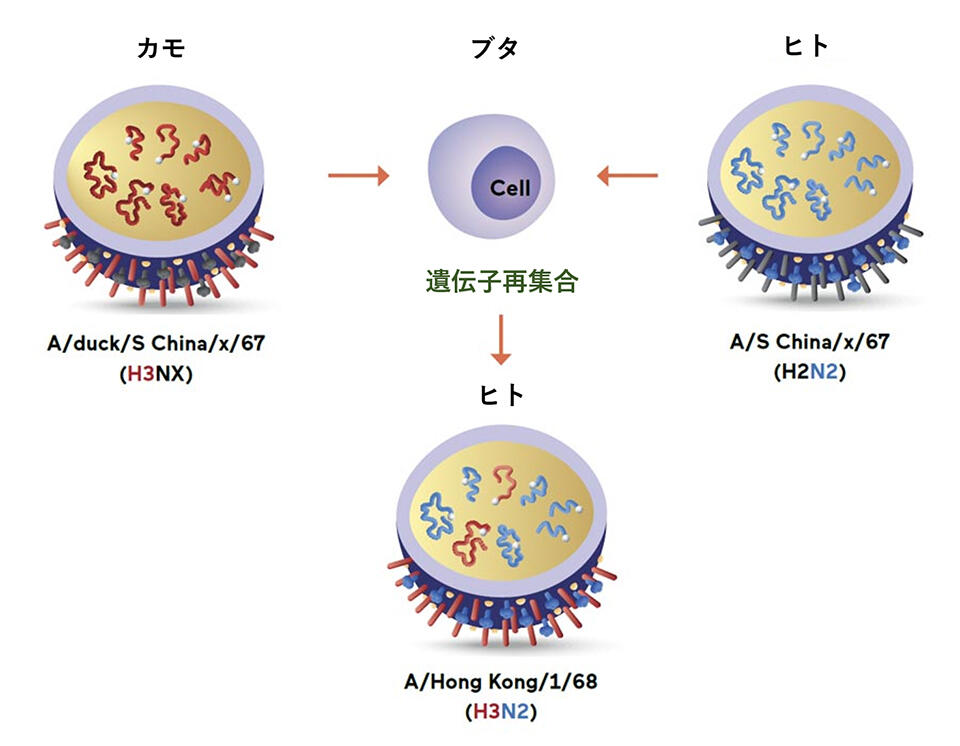 カモによって運ばれた鳥インフルエンザウイルス(H3NX)がアヒルやガチョウを介してブタに感染し、同時にヒトのH2N2型のインフルエンザに感染したことで、1968年の香港かぜのパンデミックインフルエンザウイルスが産生されたことを示す。
カモによって運ばれた鳥インフルエンザウイルス(H3NX)がアヒルやガチョウを介してブタに感染し、同時にヒトのH2N2型のインフルエンザに感染したことで、1968年の香港かぜのパンデミックインフルエンザウイルスが産生されたことを示す。インフルエンザにまつわる誤解を解く
さらに、喜田教授は「ウイルス自体は、毒素ではない」と言います。「体内でウイルスが増殖すると、自然免疫システムが反応することで症状がでます。この免疫反応が過剰になると、発熱や深刻な症状が現れるのです。重篤なケースの多くでは、血栓や血管透過性増大により血管が損傷して、子どもに見られる脳症や、多臓器不全になってしまいます」。
喜田教授は、パンデミックインフルエンザに対しても、季節性インフルエンザと同じ対応を取ることが不可欠だと言います。それには、季節性インフルエンザ用のワクチンの性能を向上させることが喫緊の課題。それに向けて、ワクチンの効き目が弱いスプリットワクチンに代わる全粒子ワクチンの導入を加速させたいと言います。
喜田教授はインフルエンザウイルスのライブリー化にも取り組んでいます。カモのフンから集めた鳥インフルエンザウイルスをライブラリー化し、ワクチン開発に必要なウイルス株をいつでも使えるようにしています。ライブラリーには、144通りの全てのHA・NA亜型の組み合わせからなる、4,600以上の鳥インフルエンザウイルス株が保管されています。これらのウイルスの病原性や抗原性、増殖性、遺伝子についての情報を分析してデータベース化し、ウェブサイトで公表しています。(https://virusdb.czc.hokudai.ac.jp/)
「データベースの特許申請をすべきという話もありましたが、断っています。必要な全ての人にデータベースを提供するのが私達の責務だと思っています。一人の研究者だけでできることには限りがありますから」と、喜田教授は研究第一主義者らしいコメントで結んでくれました。
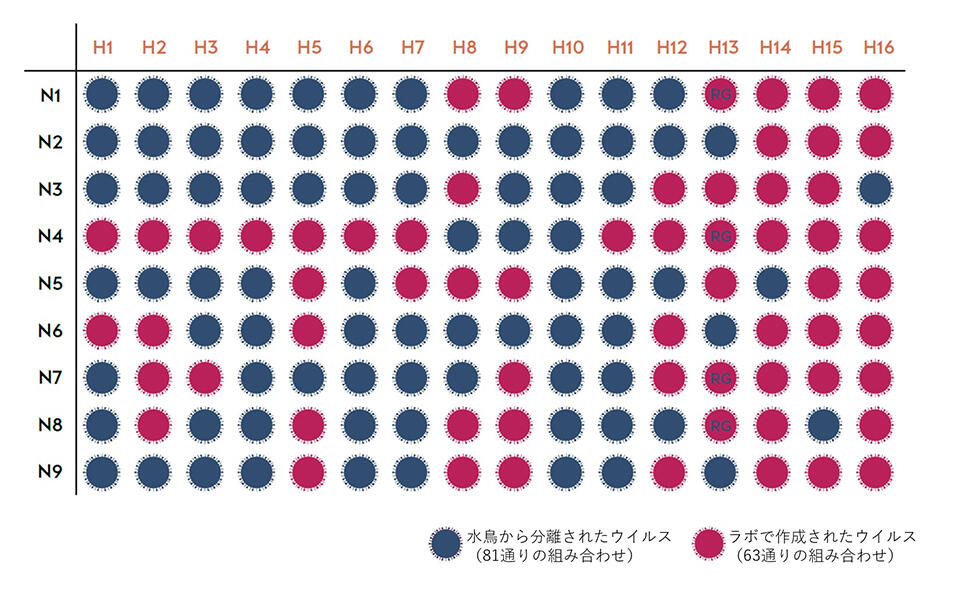 パンデミックインフルエンザのワクチン株候補ライブラリー:黒で表示されたウイルスは水鳥から分離されたもので(81通りの組み合わせ)、赤で表示されたものは研究室で作成されたもの(63通りの組み合わせ)。ライブラリーには、144のHAとNAの亜型の全ての組み合わせからなる、4,600以上の鳥インフルエンザウイルス株が保管されている。
パンデミックインフルエンザのワクチン株候補ライブラリー:黒で表示されたウイルスは水鳥から分離されたもので(81通りの組み合わせ)、赤で表示されたものは研究室で作成されたもの(63通りの組み合わせ)。ライブラリーには、144のHAとNAの亜型の全ての組み合わせからなる、4,600以上の鳥インフルエンザウイルス株が保管されている。この記事の原文は英語です
Tackling Global Issues Vol.3 Fighting the Menace of Zoonosesに掲載





